Trenutno se u svijetu razvija oko 165 različitih vakcina protiv koronavirusa. Glavne vrste vakcina uključuju vektorske vakcine, deaktivirane vakcine, vakcine osnovane na nukleinskim kiselinama (DNA i mRNA) i vakcine u osnovi kojih su rekombinirani proteini.
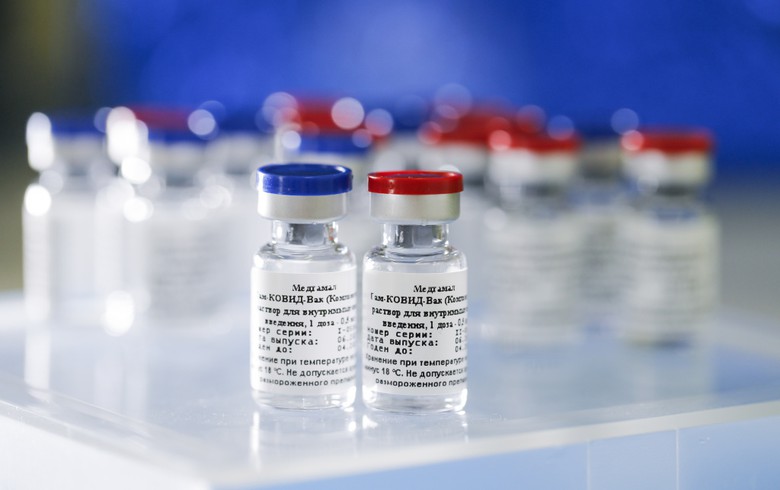
Ruska vakcina je na bazi adenovirusnog vektora. Ministarstvo zdravlja je 11. augusta registrovalo ovu vakcine i postala je prva vakcina protiv novog koronavirusa SARS-Cov-2 na tržištu. Ovaj događaj je takozvani “trenutak Sputnika” za svjetsku zajednicu.
Vakcina Sputnik V već je registrovana u više od 20 zemalja i teritorija: Rusija, Bjelorusija, Argentina, Srbija, Bolivija, Alžir, Palestina, Venezuela, Paragvaj, Turkmenistan, Mađarska, UAE, Pakistan, Iran, Gvineja, Tunis, Jermenija, Meksiko, Nikaragva, Libanon, Bosna i Hercegovina, Mijanmar, Mongolija, Bahrein, Crna Gora, Kazahstan.
Više od 31.000 dobrovoljaca učestvovalo je u kliničkom ispitivanju Sputnik V nakon registracije u Rusiji.
Ruski fond za izravna ulaganja (RDIF) zajedno sa partnerima i proizvođačima neprekidno povećavaju obim proizvodnje vakcina. Cijena jedne doze vakcine Sputnik V za strana tržišta bit će cca.16,16 KM (Sputnik V je vakcina s dvije doze). Lofilizirani (suhi) oblik vakcine može se čuvati između +2 i +8 stepeni Celzijusa, što olakšava isporuku širom svijeta, uključujući i teško dostupna područja.
„Proizvođač je uspio osigurati stabilnost vakcine, pod uslovom da se tečni oblik transportuje i čuva na temperaturama od +2 do +8 stepeni, što je potvrđeno stručnim pregledom. Ovaj hladni režim je standardni za čuvanje imunobioloških preparata ”, rekao je ministar zdravlja Ruske Federacije Mihail Muraško.
Vakcinu za opskrbu svjetskim tržištem proizvodit će međunarodni partneri RDIF-a u Indiji, Brazilu, Kini, Južnoj Koreji i drugim zemljama.
Vakcina je dobila ime po prvom sovjetskom svemirskom satelitu. Pokretanje Sputnika 1 1957. godine dalo je novi zamah istraživanju svemira širom svijeta, stvarajući tzv. “trenutak Sputnika” za svjetsku zajednicu.
Kako djeluju adenovirusne vektorske vakcine?
“Vektori” su nosioci koji mogu dostaviti genetski materijal iz drugog virusa u ćeliju. U ovom slučaju uklanja se genetski materijal adenovirusa koji uzrokuje infekciju i ubacuje se materijal s proteinskim kodom iz drugog virusa, u ovom slučaju sa šiljaka koronavirusa. Ovaj novi element siguran je za organizam, ali i pomaže imunološkom sistemu da reaguje i stvori antitijela koja štite od infekcije.
Vektorska tehnološka platforma zasnovana na adenovirusu pojednostavljuje i ubrzava stvaranje novih vakcina modifikujući izvorni vektor nosača genetskim materijalom iz novonastalih virusa, što omogućava proizvodnju novih vakcina po strogom rasporedu. Takve vakcine izazivaju snažan odgovor ljudskog imunološkog sistema.
Adenovirusni vektori smatraju se potpuno sigurnim i ujedno i najprikladnijim za genetsku modifikaciju. Vektor je virus kojem nedostaje gen za reprodukciju, tako da ne predstavlja opasnost od zaraze za organizam. Naučnici koriste vektore za transport genetskog materijala iz drugog virusa protiv kojeg se vakciniše u ćeliju.
Nakon izbivanja pandemije, ruski istraživači izvukli su fragment genetskog materijala novog koronavirusa SARS-Cov-2, koji kodira informacije o strukturi proteina virusa (proteina koji čini “krunu” virusa i odgovoran je za njeno vezanje na ljudske ćelije), te ga umetnuli u već poznati adenovirusni vektor za isporuku u ljudsku ćeliju, stvarajući tako prvu vakcinu u svijetu protiv SARS-Cov-2.
Gen koji kodira S-protein ubacuje se u sastav svakog vektora, a trnje čini “krunu”, po kojoj je virus i dobio ime. Uz pomoć trnja virus SARS-Cov-2 ulazi u ćeliju virusa.
Šta su adenovirusi?
Adenovirusi su porodica virusa koji sadrže DNK kičmenjaka i lišeni su omotača lipoproteina. Adenovirusi imaju promjer 70-90 nm i sadrže jednostruki dvolančani molekul DNA dužine 34-36 kb. Najpoznatiji su adenovirusi koji uzrokuju akutne respiratorne infekcije. Naziv dolazi od njihove početne izolacije od adenoida.
Adenovirusi se koriste kao virusni vektor za gensku terapiju zbog njihove sposobnosti da se repliciraju u djeljivim i nedjeljivim ćelijama.
U Kini se adenovirusi koriste u liječenju karcinoma.
Kako bi osigurali dugoročni imunitet, ruski naučnici predložili su upotrebu dvije različite vrste adenovirusih vektora za prvu i drugu vakcinaciju, pojačavajući učinak vakcine.
Prva vakcinacija
Vektor s genom koji kodira S-protein koronavirusa ulazi u ćeliju. Organizam sintezira S-protein, kao odgvor na to započinje proizvodnja imuniteta.
Druga vakcinacija
Nakon 21 dana javlja se revakcinacija. Vakcina zasnovana na drugom, nepoznatom organizmu, adenovirusnom vektoru stimulira imunološki odgovor organizma i pruža dugoročni imunitet.
Upotreba dva vektora jedinstvena je tehnologija Centra navanog po N.F. Gamaleya i razlikuje rusku vakcinu od ostalih vakcina zasnovanih na adenovirusnim vektorima koji se razvijaju u svijetu.
Klinička ispitivanja
Prije nego što su započeli klinička ispitivanja, vakcina je u potpunosti prošla sve faze pretkliničke efikasnosti i ispitivanja sgurnosti, koje su uključivale eksperimente na različitim vrstama laboratorijskih životinja, uključujući dvije vrste primata.
Klinička ispitivanja vakcine 1. i 2. faze završena su 1. augusta 2020. Svi dobrovoljci dobro su podnosili testove, nisu zabilježeni neočekivane i ozbiljne neželjne posljedice, vakcina je inducirala svrstanje visokih antitijela i ćelijski imunološki odgovor. Visoka efikasnost vakcine potvrđena je testovima visoke preciznosti na antitijela u krvnom serumu dobrovoljaca (uključujući analizu antitijela koja neutrališu koronavirus), kao i sposobnošću imunoloških ćelija dobrovoljaca da se aktiviraju kao odgovor na S-protein koronavirusa, što ukazuje na stvaranje i antitijela i ćelijskog imunog odgovora kao rezultat vakcinacije.
Aktivna supstanca vakcine Sputnik V i način njene upotrebe imaju patentnu zaštitu na teritoriji Rusije, koja pripada Nacionalnom istraživačkom centru zs epidemiologiju i mikrobiologiju.
Predklinička ispitivanja
Predklinička ispitivanja rekombinantne vakcine na toksičnost, sigurnost, imunogenost i zaštitnu efikasnost kod velikih i malih životinja obavljena su u Istraživačkom institutu za mikrobiologiju Ministarstva odbrane Ruske Federacije.
Ispitivanja su provedena na dvije vrste osjetljivih sisara: zlatnom sirijskom hrčku i dvije vrste primata. Postignuća osoblja vojnog istraživačkog instituta pomogla su da se skrati predklinička procjena sigurnosti i efikasnosti vakcine. Konkretno, korištena je metodologija za kvantitativnu procjenu patogena i laboratorijski model za reprodukciju teške akutne respiratorne bolesti razvijen u Istraživačkom institutu.
Klinička ispitivanja faze I / II “Gam-COVID-Vac”
Ova faza kliničkih ispitivanja otvorena je studija sigurnosti, podnošljivosti i imunogenosti Gam-COVID-Vac (pod ovim nazivom je registrovana vakcina). Dana 16. juna 2020. godine, Ministarstvo zdravlja Ruske Federacije izdalo je dozvolu br. 241 za provođenje ovog kliničkog ispitivanja.
Ispitivanja tečne vakcine provedena su u Glavnoj vojnoj kliničkoj bolnici N.N.Burdenko (GVKG). U ispitivanju je sudjelovalo 38 dobrovoljaca. U prvoj fazi ispitivanja (faza I), sigurnost, podnošljivost i imunogenost svake komponente cjepiva testirane su odvojeno: prvoj grupi od 9 ljudi ubrizgana je komponenta I, drugoj grupi od 9 osoba ubrizgana komponenta II. U drugoj fazi (faza II), ispitivanje je provedeno prema obnoviteljskoj shemi: 20 ljudi je dobilo injekcije komponente I, a nakon 21 dana – komponente II. Svi dobrovoljci razvili su visoke titre antitijela na COVID-19. Niko od njih nije imao ozbiljnih komplikacija imunizacije.
Klinička ispitivanja faze I / II “Gam-COVID-Vac-Lyo”
Ova faza kliničkih ispitivanja otvorena je studija sigurnosti, podnošljivosti i imunogenosti Gam-COVID-Vac Lyo. Dana 16. juna 2020. godine, Ministarstvo zdravlja Ruske Federacije izdalo je dozvolu br. 242.
Liofilizirana (suha) vakcina testirana je na Prvom moskovskom državnom medicinskom univerzitetu I.M.Sechenov. U ispitivanju je sudjelovalo 38 dobrovoljaca. U prvoj fazi ispitivanja (faza I), sigurnost, podnošljivost i imunogenost svake komponente cjepiva testirane su odvojeno: prvoj grupi od 9 ljudi ubrizgana je komponenta I, drugoj grupi od 9 osoba ubrizgana komponenta II. U drugoj fazi (faza II), ispitivanje je provedeno prema obnoviteljskoj shemi: 20 ljudi je dobilo injekcije komponente I, a nakon 21 dana – komponente II. Svi dobrovoljci razvili su visoke titre antitijela na COVID-19. Niko od njih nije imao ozbiljnih komplikacija imunizacije.
Klinička ispitivanja faze III (nakon registracije)
Ova faza je randomizirano, dvostruko slijepo, s placebom kontrolirano, multicentrično kliničko ispitivanje s paralelnim određivanjem efikasnosti, sigurnosti i imunogenosti kombiniranog vektorskog cjepiva “Gam-COVID-Vac” u preventivnom liječenju SARS-CoV-2 infekcija. Dozvolu za provođenje ovog CT-a pod brojem 450 izdalo je Ministarstvo zdravlja Ruske Federacije 25. avgusta 2020. godine, nakon registracije vakcine. Planirano je da 40 000 volontera starih 18 i više godina učestvuje u ovom ispitivanju. Nakon kontrole prisutnosti virusa, sudionici su, prema dizajnu ispitivanja, trebali biti randomizirani u dvije grupe – studijsku grupu od 30 000 dobrovoljaca koji su primali kombiniranu vektorsku vakcinu Gam-COVID-Vac protiv virusa SARS-CoV-2 i kontrola grupe od 10 000 dobrovoljaca koji su primali placebo.
Istraživanje je započelo 26. avgusta u Moskvi. Za provođenje ispitivanja vakcina bilo je uključeno 25 medicinskih organizacija grada. Zdravstveno praćenje učesnika mora trajati najmanje 6 mjeseci. Za to je stvorena posebna mobilna aplikacija sa dnevnikom samopromatranja, a neki su učesnici dobili elektronske narukvice za mjerenje krvnog pritiska i tjelesne temperature. Učestvovali volonteri stariji od 18 godina. Odabrani su samo oni koji su imali negativne rezultate na HIV, hepatitis B i C i sifilis, PCR test na SARS-CoV-2 i testove na IgG i IgM na antigene, bez zaraznih bolesti i kontakta sa zaraženim koronavirusom tokom 14 dana, bez bilo kakva cijepljenja izvršena u roku od mjesec dana prije prve doze.
Privremeni rezultati studije objavljeni su 2. februara 2021. u časopisu The Lancet. Analizom primarnih rezultata obuhvaćeno je 19.866 ljudi koji su primili vakcinu ili placebo. Nakon 21. dana studije, 16 od 14.964 sudionika u cijepljenoj grupi (0,1%) i 62 od 4902 sudionika u placebo grupi (1,3%) potvrdilo je COVID-19.
Epidemiološka efikasnost vakcine bila je 91,6% + 3,6%
−5,7% (margina greške ukazuje na 95% intervala pouzdanosti zbog statističkog vjerovatnosnog širenja). 97 slučajeva COVID-19 (63 u vakcinisanoj grupi i 34 u placebo grupi) zabilježeno je prije 21 dan nakon prve doze, odnosno prije pojave imuniteta izazvanog cjepivom, i nisu bili uključeni u analizu.
Epidemiološka efikasnost za učesnike starije od 60 godina iznosi 91,8% (95% interval pouzdanosti od 67,1% do 98,3%) i ne razlikuje se statistički od efikasnosti za cijelu grupu. Nije bilo slučajeva umjerenog ili ozbiljnog COVID-19 u grupi cijepljenih, bilo ih je 20 u placebo grupi; to znači efikasnost protiv takvih oblika bolesti u 95% intervalu pouzdanosti od 94,4% do 100%. Nesklad između vjerovatnoće bolesti u cijepljenoj i placebo grupi na vremenskom rasporedu počinje oko 18. dana nakon prve doze. 45 učesnika (0,3%) od 16.427 u vakcinisanoj grupi i 23 (0,4%) od 5435 u placebo grupi prijavilo je ozbiljne neželjene događaje, ali neovisni odbor za praćenje podataka potvrdio je da nisu povezani sa vakcinom.
Tokom studije, bilo je četiri smrtna slučaja sudionika: 3 među 16.427 cijepljenih i 1 među 5435 u placebo grupi. U grupi cijepljenih, jedna smrt povezana je s prijelomom torakalnog kralješka, dvije s COVID-19. Oni koji su umrli od COVID-19 razvili su simptome 4. i 5. dana nakon prve doze vakcine (dakle, oba su učesnika zaražena prije uključivanja u studiju, uprkos negativnom rezultatu PCR-a), obojica su imala popratne bolesti (kardiovaskularne i endokrinološke , odnosno). U placebo grupi, sudionik je umro od hemoragičnog moždanog udara.
Faza II, klinička studija sa dobrovoljcima starijim od 60 godina
Ovo je otvorena studija o sigurnosti, podnošljivosti i imunogenosti cjepiva Gam-COVID-Vac protiv COVID-19 s dobrovoljcima u starosnoj grupi 60+. Dozvolu br. 566 za provođenje ovog CT-a izdalo je Ministarstvo zdravlja Ruske Federacije 13. oktobra 2020. godine. U istraživanju je učestvovalo 110 ljudi.